选择题
总计50分,每题2分
1.(2023·无锡高一检测)下列各物质,按单质、化合物、混合物顺序排列的是( )
A.铝、纯碱、盐酸 \(~~~~~~~~~~~~~~~~~\) B.红磷、熟石灰、水
C.石墨、稀硫酸、胆矾 \(~~~~~~~~~~~~~~~~~\) D.石灰水、干冰、空气
2.(2022河北武安第一中学高一月考)下列液体,不会丁达尔效应的分散系是( )
①稀牛奶 ②纯水 ③淀粉溶液 ④硫酸钠溶液 ⑤向沸水中滴入FeCl3饱和溶液形成红褐溶液体 ⑥肥皂水
A.②④ B.③④ C.②④⑥ D.④
3.(2022·泰安高一检测)物质M在水溶液中分生电离:M=\(X^{2+}\)\(+2Y^-\),下列判断正确的是( )
A.M可能是酸 \(~~~~~~~~~~~~~~~~~\) B.\(X^{2+}\)一定是金属离子
C.\(Y^-\)一定是\(OH^-\) \(~~~~~~~~~~~~~~~~~\) D.M一定属于盐
4.(2023·上海高一检测)在酸性溶液中能大量共存且溶液为无色透明的离子组是( )
A.\(K^+\)、\(MnO^{4-}\)、\(Na^+\)、Cl
B.\(K^+\)、\(Na^+\)、\(NO^{3-}\)、\(SO_3^{2-}\)
C.\(Ba^{2+}\)、\(Na^+\)、\(NO^{3-}\)、\(SO_4^{2-}\)
D.\(Mg^{2+}\)、\(Na^+\)、\(Cl^-\)、\(SO_4^{2-}\)
5.(2022湖南衡阳高一期中)下列反应的离子方程式书写正确的是( )
A.向氢氧化铜悬浊液中加入稀酸酸:\(H^++OH^-=H_20^-\)
B.稀硫酸滴在铜片上:\(Cu+2H^+=H^2↑+Cu^{2+}\)
C.向氧化亚铁中滴加稀盐酸:\(FeO+2H^+=H_20+Fe^{2+}\)
D.\(Fe_2(SO_4)_3\)溶液与NaOH溶液反应:\(2Fe^{3+}+3OH^-=2Fe(OH)_3↓\)
6(许以诺).已知氧化性:\(Br_2>Fe^{3+}>I_2\),还原性:\(I^->Fe^{2+}+Br^-\),则下列反应不能发生的是
A.\(Br_2+2I^- =2Br^- +I_2\) \(~~~~~~~~~~~~~~~~~\) B.\(Br_2+2Fe^{2+}=2Br^-+2Fe^{3+}\)
C.\(2Fe^{3+}+2I^-=2Fe^{2+}+I_2\) \(~~~~~~~~~~~~~~~~~\) D.\(2Fe^{3+}+2Br^-=2Fe^{2+}+Br_2\)
7(许以诺).“氯气对水一心一意,水偏弄成三分四离”其中“三分四离”指的是新制氯水中的七种微粒。下列实验现象和结论一致的是 ()
A.新制氯水使紫色石蕊溶液先变红后褪色,说明有氯气分子和\(H^-\)存在。
B.向新制氯水中加入饱和\(NaHCO_3\)溶液,有无色气体产生,说明有HCIO存在。
C.向新制氯水中加入饱和\(NaHCO_3\)溶液,有无色气体产生,说明氯气和水反应生成了HCI。
D.向新制氯水中加入NaOH溶液,氯水黄绿色消失,说明氯水中的氯气分子与氢氧化钠直接反应。
8(许以诺).(2022·安徽合肥一中高一期未)一个氯原子的质量为a g,一个12C的质量是b g,用NA表示阿伏加德罗常数的值,下列说法正确的是()
A.氯元素的相对原子质量为\(\frac{12a}{b}\)
B.氯元素的摩尔质量为\(aNA g/mol^{-1}\)
C.m g该氯原子的物质的量为\(\frac{m}{aNA}mol\)
D.n g该氯原子所含的电子数为\(\frac{17n}{aNA}\)
9(许以诺).常温下,发生下列几种反应
①\(16H^++10C1^-+2MnO^{4-}=2Mn^{2+}+5Cl_2↑+8H_2O\)
②\(2Fe^{2+}+Br_2=2Fe^{3+}+2Br^-\)
③\(2Br^-+Cl_2=Br_2+2Cl^-\)
根据上述文应。判断下列结论错误的是()
A.溶液中可发生:\(CI_2+2Fe^{2+}=2Fe^{3+}+2C1^-\)
B.\(C1_2\)在①③反应中均为氧化剂
C.氧化性强弱的顺序为\(MnO^{4-}>Cl_2﹥Br_2>Fe^{3+}\)
D. \(Mn^{2+}\)是\(MnO^{4-}\)的还原产物
10(陈李).现有氯化铵、硫酸铵和硫酸钾三种无色溶液,只用一种试剂一次区别开,则该试剂是(必要时可以加热) ( )
A. 氯化钡溶液 B.氢氧化钡溶液 C.稀盐酸 D.硝酸银溶液
11(陈李).现有10.6g碳酸钠和碳酸氢钠的固体混合物,加入足量盐酸充分反映,将所得溶液蒸干、称量,得到的固体质量可能为( )
A.10.0g B.11.7g C.12.0g D.14.0g
12(陈李).下列叙述正确的是( )
A. 氯气的性质很活泼,它与氢气混合后立即发生爆炸
B. 实验室制取氯气时,为了防止污染环境,多余的氯气用氢氧化钙溶
液吸收
C. 新制氯水的漂白性比久置氯水的强
D. 检验HCl气体中是否混有氯气的方法是将气体通入硝酸银溶液
13(陈李).下列有关化学基本概念的依据正确的是( )
A. 溶液与胶体:属于不同分散系的本质原因是能否发生丁达尔效应
B. 纯净物与混合物:是否仅含有一种元素
C. 氧化还原反应:元素化合价是否变化
D. 电解质与非电解质:物质本身的导电性
14(鲍宇宁).一定条件下,当溶液中\(XO^{4-}\)与\(H_2O_2\)分子个数比恰好为2:5时溶液\(XO^{4-}\)被还原为较低价态,则X元素化合价变为( )
A.+2 B.+3 C.+4 D.+5
15(鲍宇宁).用洁净的铂丝蘸取某无色溶液,放在无色火焰上灼烧,火焰的颜色呈黄色。下列说法错误的是( )
A.该溶液中可能含钠离子,一定没有钾离子
B.该溶液中一定含有钠离子
C.该溶液中一定没有铜离子
D.该溶液中可能含有钾离子
16(鲍宇宁).我国科学家屠呦呦发现青蒿素,它是一种用于治疗疟疾的药物。2015年十月获得诺贝尔生理学或医学奖。下列有关青蒿素(化学式:\(C_{15}H_{22}O_5\))的叙述,正确的是( )
A.青蒿素的摩尔质量为282
B.6.02×10²³个青蒿素分子的质量约为282g
C.1摩尔青蒿素的质量为282g/mol
D.282克青蒿素中含有15个碳原子
17(鲍宇宁).某白色粉末中可能含有\(Ba(NO_3)_2、CaCl_2、K_2CO_3\)进行如下实验:
①向少量粉末加入水中,震荡有白色沉淀生成
②向①的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生
③取少量的溶液滴入硝酸银溶液,有白色沉淀生成
依据实验现象下列关于白色粉末的判断,正确的是
A.只含有\(K_2CO_3\)
B.一定含有\(K_2CO_3、CaCl_2\) 和\(Ba(NO_3)_2\)
C.一定含有\(K_2CO_3\)和\(CaCl_2\),可能含有\(Ba(NO_3)_2\)
D.一定含有\(K_2CO_3\),还含有\(CaCl_2\)和\(Ba(NO_3)_2\)中的一种
18(吴语歌).200℃时,11.6g二氧化碳和水蒸气的混合气体与足量的过氧化钠充分反应后固体质量增加了3.6g(如图所示),其原混合物中二氧化碳和水的质量之比是( )
A.11:8 B.22:3 C.1:9 D.21:9
19(吴语歌).下列说法不正确的是( )
A.温度相同,体积相同的氧气和氮气分子数相同
B.等温等压下,二氧化硫气体与二氧化碳气体的密度之比为16:11
C.等温等体积下,5mol氧气和2mol氮气的压强之比等于5:2
D.等温等压下,32g氧气和2g氢气的体积之比等于1:1
20(吴语歌).已知a克气体\(XY_3\)含有b个原子,设阿伏加德罗常数的值为NA气体摩尔体积为c L/mol,则该条件下11.2L该气体的质量为?
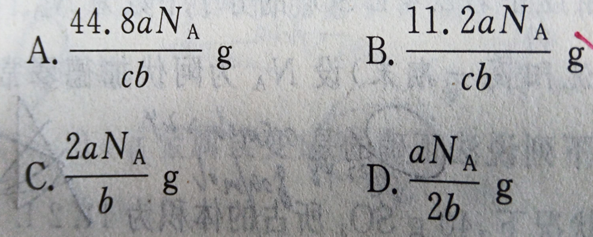
21(吴语歌).设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,2.24L乙醇中含有0.1NA个分子
B. 常温常压下,80g氩气含有的原子数为2 NA
C. 1mol过氧化钠与足量水反应产生11.2L的氧气
D. 1mol氯气与足量的铁粉反应转移的电子数目是3NA
22.(李书畅)某溶液中含有大量的下列离子:\(Fe^{3+}、NO^{3-}、K^+和M\)。四者按上述的顺序的的离子个数比为2:5:1:1,则M可能是下列中的()
A.\(Cl^-\) B.\(SO_4^{2-}\) C.\(Ca^{2+}\) D.\(Na^{+}\)
23.(李书畅)下列有关描述中不涉及氧化还原反应的是()
A.植物的光合作用 \(~~~~~~~~~~~~~~~~~\)B.钟乳石的形成
C.工业上利用活冶炼经书铜 \(~~~~~~~~~~~~~~~~~\) D.食物腐败
24.(李书畅)下列属于氧化还原反应,但是水既不做氧化剂也不做还原剂的是()
A.\(H_2O + CaO = Ca(OH)_2\)
B.\(H_2O + 2Na = 2HNO_3 + NO\)
c.\(3NO_2 + H_2O = 2NaOH + H_2↑\)
D.\(2H_2O \stackrel{电解}{{=\!=\!=}} 2H_2↑ + O_2↑\)
25.(李书畅)
填空题
总计50分
26(陈李)(10分,每空2分).某校化学兴趣小组同学猜想自来水中可能含有大量铜离子、钙离子、镁离子和某些阴离子,从而进行了三组实验:
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的碳酸钠溶液,又有白色沉淀产生;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加硝酸银溶液,也产生白色沉淀。
请回答以下问题:
( 1 )不用做实验就可排除的离子是_________________ 。
( 2 )通过实验可初步确定自来水中_____________(填“含有”或“不含有”)大量钙离子、镁离子;判断依据的离子方程式有________________________________ 。
( 3 )自来水中所含阴离子可以确定有_________________________,理由是______________________________________。
27(吴语歌)(10分,每空2分).5. 现有16g一氧化碳和二氧化碳的混合气体,在标准状况下,其体积为8.96L,请回答下列问题:
⑴该混合气体的平均摩尔质量为___________。
⑵混合气体中碳原子的个数为_____________用NA表示阿伏加德罗常数的值)。
⑶将混合气体依次通过如图所示装置最后收集在气球中(体积在标准状况下测定)。
①气球中收集到的气体的质量为_____________________。
②气球中收集到的气体中电子总数为____________。
(用NA表示,假设气体全部进入气球中)。
③气球的体积为_____________L(忽略气球弹性的影响)
④若将混合气体通入足量的过氧化钠中,转移的电子数为 ______________(用NA表示)。
28(李书畅)(8分,每空2分).
29(鲍宇宁)(10分,除了最后一个空每个空1分,最后一个空2分).

30(马一鉴)(10分).粥籽糕是一个很好学的学生,一天,他遇到了一个问题,求出10.6g\(Na_2CO_3\)与稀盐酸完全反应的\(CO_2\)质量,他列出了如下方程:
\(Na_2CO_3\) ~ \(CO_2\)
\(106\) \(~~~~~\) \(44\)
\(\frac{m(Na_2CO_3)}{106} = \frac{m(CO_2)}{44}\)①
\(m(CO_2) = 4.4g\)
他突然很好奇为什么可以使用①处的等式,他的同学无语来用物质的量相关的知识为他解答了疑惑:_____________________________________________________________________________________________________________________________________________________________________________________________________________________(5分)
他恍然大悟,开始了新的探索。
无语来和粥籽糕在一起做一道绝世好题,两人都想比对方先做出这道题,请你帮助无语来做出这道题:
现有一个密闭的容器横放在桌面上,容器的正中间有一个活塞(活塞两边相当于密封),左边的气体为一氧化碳和氧气,右边的气体为甲烷和氧气,加热点燃两边的气体,完全反应冷却至室温后(活塞与容器壁之间无摩擦),活塞处于3:2的位置(左:右),求两边气体反应的可能比例(液体体积忽略不计)。通过一些限定条件,无语来得出了一下可能,请你帮他判断哪些可能(一氧化碳:氧气、甲烷:氧气)是错误的__________________:(全对得5分,选错不得分,漏选得2分)
A.1:1、4:5
B.2:1、1:1
C.4:7、6:5
D.1:9、1:9